全程導醫網 徐州傳染頻道:據《中共中央辦公廳、國務院辦公廳印發〈關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見〉的通知》(廳字〔2017〕42號)和《國務院關于修改〈醫療器械監督管理條例〉的決定》(國務院令第680號)規定,醫療器械臨床試驗機構由資格認定改為備案管理。自2019年1月1日起所有從事醫療器械臨床試驗的臨床研究人員若要開展試驗,必須在經過醫療器械臨床試驗資格備案的醫療機構內進行。

為加強徐州市傳染病醫院臨床試驗機構能力建設,提升臨床試驗發展水平,形成完善的臨床試驗研究和服務體系,促進該院醫學科研能力建設,醫院領導高度重視,鼓勵臨床醫生積極申報參與藥品/醫療器械臨床試驗研究。在醫院領導的推動下,該院GCP機構辦公室開始積極準備備案所需的各種材料,于2019年10月16日獲得國家藥物臨床試驗機構認定資格,認定專業為:肝炎專業、結核病和性傳播疾病專業。

新型冠狀病毒疫情期間,針對疫情防控,我院藥物臨床試驗機構為配合做好疫情防控工作,結合該院實際情況,切實保障受試者、GCP相關從業人員的生命健康安全,對本院的臨床試驗進行了調整,相關工作應與各級政府及醫院對新型冠狀病毒肺炎疫情的防控要求保持一致。遏制新型冠狀病毒肺炎疫情蔓延,國家藥監局開通了新型冠狀病毒核酸檢測試劑盒快速審批通道。為積極推動醫院參與新型冠狀病毒診斷試劑研發,臨床一線,臨床試驗機構、倫理委員會開啟與新冠肺炎相關項目綠色通道。
該院院黨委書記親自掛帥,藥物(器械)臨床試驗機構、倫理委員會召開緊急會議,積極動員專業科室培訓學習相關法律法規,邀請徐州市科技服務行業協會來院授課指導,各位參與人員在抗擊疫情艱苦的條件下,完滿地完成了備案申請,肝炎科、結核病科,感染科和檢驗科,獲得器械(含體外診斷試劑)臨床試驗開展資格。備案號:械臨機構備202000037。
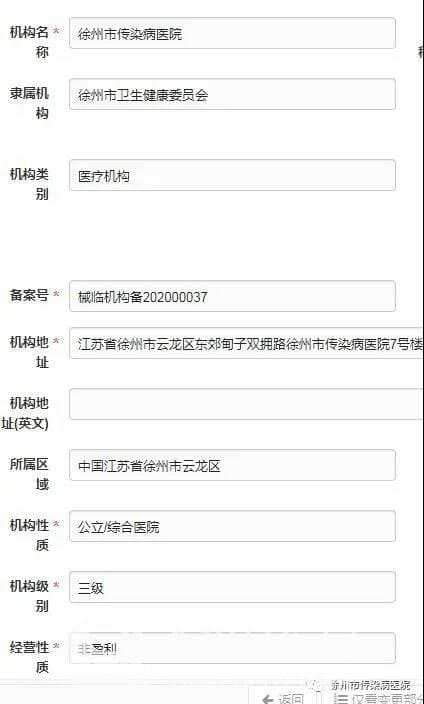
醫療器械臨床試驗機構備案,為該院GCP機構的發展壯大邁出了重要而堅實的一步,更為該院抗擊新型冠狀病毒肺炎增添了一件強力的武器。
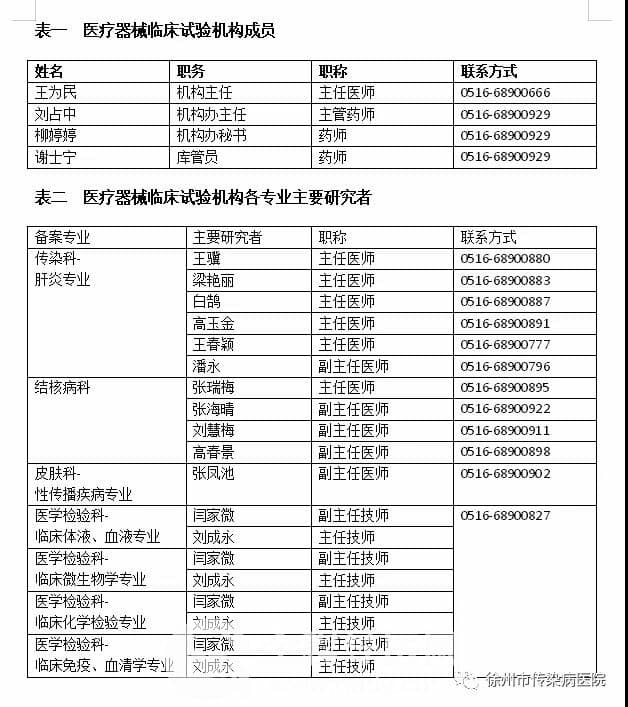
完成備案后,徐州市傳染病醫院可以開展包括體外診斷試劑和治療等醫療器械的臨床試驗。主要有:物理治療器械;輸血、透析和體外循環器械;醫療器械消毒滅菌器械;注輸、護理和防護器械;臨床檢驗器械;體外診斷試劑等。
徐州健康熱線:0516-85707122





